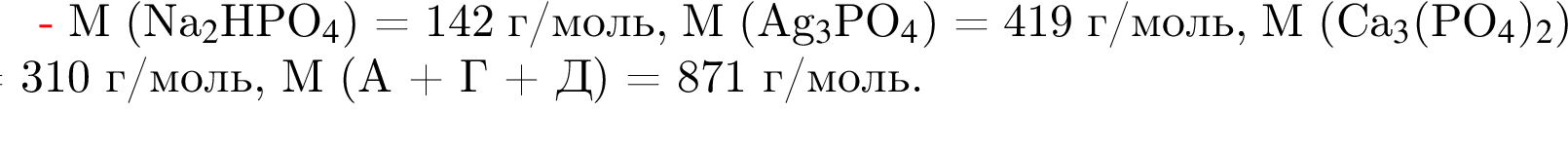Анионом является частица, формула которой:
Число протонов в ядре атома ![]() равно:
равно:
Число полностью заполненных энергетических подуровней на внешнем энергетическом уровне атома элемента с порядковым номером 10 в основном состоянии равно:
Элемент, имеющий распределение электронов в атоме по энергетическим уровням 2, 8, 3, расположен в периодической системе:
В сосуд, показанный на рисунке, методом вытеснения воздуха (Мr = 29) можно собрать газ:
Наименьшее значение степени окисления атомы хлора имеют в соединении:
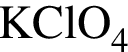
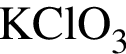
Укажите признаки, соответствующие веществу, химическая формула которого ![]() :
:
а) его водный раствор называется соляной кислотой
б) относится к многоосновным кислотам
в) относится к бескислородным кислотам
г) образует соли — хлораты
Прибор, изображенный на рисунке, используют для выделения вещества из неоднородной смеси методом:
НЕЛЬЗЯ приготовить насыщенный водный раствор при комнатной температуре:
Для получения серебра из водного раствора нитрата серебра (I) целесообразно использовать металл:
Двухосновная бескислородная кислота образуется при взаимодействии в водном растворе веществ:
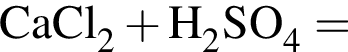
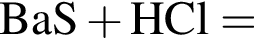
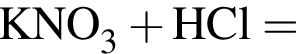
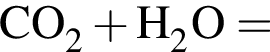
Основные свойства высших оксидов предложенных элементов монотонно усиливаются в ряду:
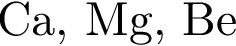
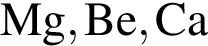
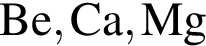
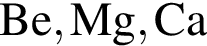
В водном растворе дигидрофосфат натрия взаимодействует с:
а) хлоридом калия;
б) гидроксидом натрия;
в) фосфорной кислотой;
г) серной кислотой.
Укажите правильные утверждения относительно вещества, химическая формула которого 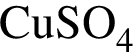 :
:
а — слабый электролит
б — имеет название сульфат меди(I)
в — является средней солью
г — мольное отношение катионов и анионов в формульной единице 1 : 1
Укажите вещества, водные растворы которых содержат одинаковые ионы (гидролиз веществ и диссоциацию воды не учитывайте):
а) 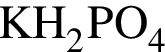
б) 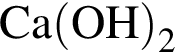
в) 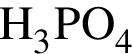
г) 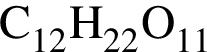
Исходные концентрации веществ А и В, участвующих в одностадийной реакции А + В = С, равны соответственно 0,68 моль/дм3 и 1,2 моль/дм3. Через 40 с после начала реакции концентрация вещества А снизилась до 0,28 моль/дм3. Средняя скорость (моль/дм3 · с) данной реакции и концентрация вещества В (моль/дм3) через 40 с после начала реакции равны соответственно:
Общее число веществ из предложенных — 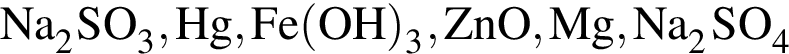 с которыми при комнатной температуре реагирует разбавленная азотная кислота равно:
с которыми при комнатной температуре реагирует разбавленная азотная кислота равно:
Железный гвоздь погрузил в разбавленный водный раствор вещества Х. При этом масса гвоздя НЕ изменилась. Веществом Х является:
Массовая доля металла в оксиде MeO равна 60,0%. Для этого металла справедливо утверждение:
Массовая доля металла в оксиде состава ![]() равна 71,4 %. Выберите утверждения, характеризующие металл:
равна 71,4 %. Выберите утверждения, характеризующие металл:
а) НЕ восстанавливается водородом из оксида
б) используется в изготовлении ювелирных украшений
в) реагирует с водой (20 °C)
г) в соединениях имеет переменную валентность
В закрытом сосуде постоянного объёма установилось равновесие

Затем температуру повысили. Для новой равновесной системы по сравнению с первоначальной верными являются утверждения:
а) давление в системе уменьшилось
б) давление в системе увеличилось
в) израсходовался водород количеством вдвое меньшим, чем образовалась йодоводорода
г) количество йода увеличилось
В закрытом сосуде протекает химическая реакция А + 2В = 2С + D. До начала реакции молярная концентрация вещества В равнялась 1 моль/дм3, а вещества D — 0 моль/дм3. Через сколько секунд концентрации веществ В и D сравняются, если скорость образования вещества D составляет 0,04 моль/дм3 · с (все вещества — газы, объем сосуда постоянный)?
Водный раствор дигидрофосфата натрия вступает в реакцию со всеми веществами, формулы которых:
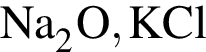
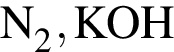
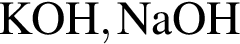
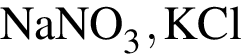
Окислительно-восстановительной реакцией является реакция, схема которой:
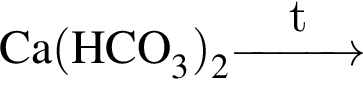
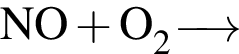
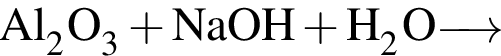
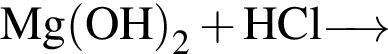
К уменьшению ![]() водного раствора приведёт:
водного раствора приведёт:
Дана схема превращений
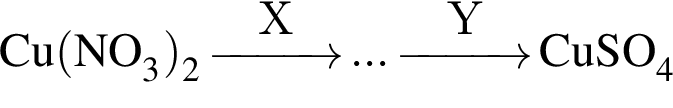
Обе реакции являются окислительно-восстановительными. Укажите возможные реагенты ![]() и
и ![]() :
:
а — магний и серная кислота (конц.)
б — гидроксид натрия и серная кислота
в — цинк и сульфат ртути(II)
г — карбонат калия и серная кислота
Укажите формулу соединения, которое вступает в реакции поликонденсации:
Укажите процесс, одним из продуктов которого является кислород:
При взаимодействии бутена-2 с хлороводородом образуется вещество, в молекуле которого число атомов равно:
ацетилен 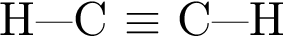 взаимодействует с хлороводородом в отношении химического количества 1:1. При этом:
взаимодействует с хлороводородом в отношении химического количества 1:1. При этом:
а) связь между атомами укорачивается
б) протекает реакция замещения
в) валентный угол 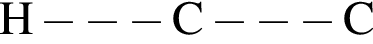 уменьшается
уменьшается
г) число ![]() -связей увеличивается
-связей увеличивается
Вещество, которое НЕ вступает в реакцию гидрирования, — это:
К классу спиртов относится основной органический продукт превращений:
а — 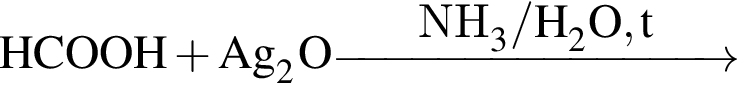
б — 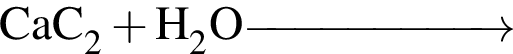
в — 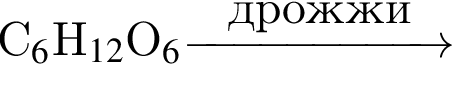
г — 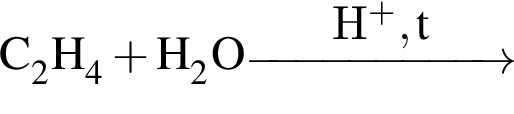
Укажите схему реакции присоединения согласно классификации органических реакций:

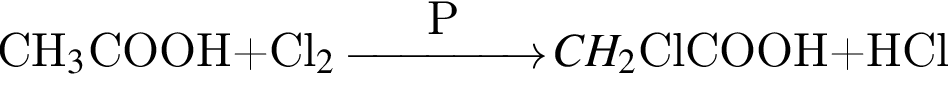
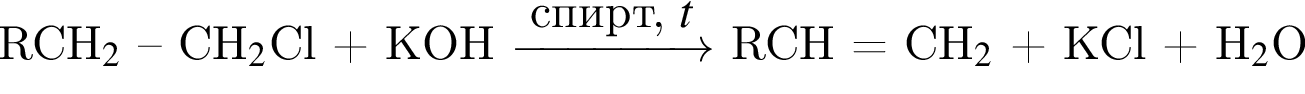
Альдегид образуется по схеме:
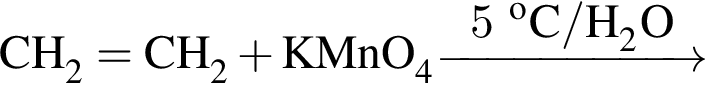
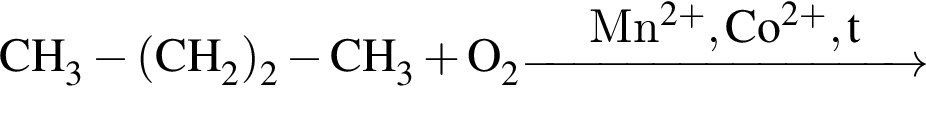
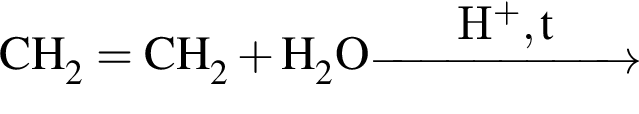
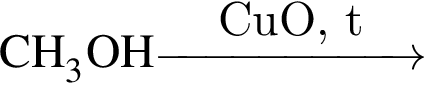
Углеводу НЕ соответствует формула:
Укажите формулу ![]() -глюкозы:
-глюкозы:
Дипептид образуется при взаимодействии 2-аминопропановой кислоты с веществом, название которого:
В промышленности реакцию полимеризации используют для получения:
Альдегид А имеет молярную массу меньше 31 г/моль, при гидрировании образует вещество Б молярной массой больше 31 г/моль. При окислении А может быть получено органическое вещество B, водный раствор которого окрашивает метилоранж в красный цвет. При нагревании Б с B в присутствии серной кислоты образуются легкокипящая жидкость Г и неорганическое вещество Д. Укажите сумму молярных масс (г/моль) веществ B и Г.
Выберите верные утверждения относительно бензола:
Ответ запишите в виде последовательности цифр в порядке возрастания, например: 245 .
Укажите сумму молярных масс (г/моль) органического вещества ![]() и медьсодержащего вещества
и медьсодержащего вещества ![]() , образующихся в результате следующих превращений:
, образующихся в результате следующих превращений:
Смесь алканов массой 94 г полностью сожгли в кислороде. На сжигание было затрачено 246,4 дм3 кислорода (н. у.). Укажите массу (г) воды, полученной при сгорании смеси алканов.
B четырех пронумерованных пробирках находятся органические вещества.
О них известно следующее:
— в пробирке № 1 — кристаллическое вещество (20 °C), реагирующее с водным раствором гидроксида натрия
— содержимое пробирок № 2 и № 3 — жидкости (20 °C), которые неограниченно растворяются в воде
— вещество в пробирке № 3 взаимодействует со свежеприготовленным в щелочной среде гидроксидом меди(П) с образованием раствора ярко-синего цвета.
Установите соответствие между названием органического вещества и номером пробирки, в которой находится указанное вещество.
А) этанол
Б) гексан
В) этиленгликоль
Г) фенол
1
2
3
4
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца, например: А1Б4B2ГЗ.
Простое газообразное вещество А желто-зеленого цвета с резким запахом реагирует с металлом Б, в результате чего получается вещество В. Газ А имеет плотность (н. у.), равную 3,17г/дм3. Химический элемент, образующий Б, в соединениях имеет валентность II, а избыток его катионов обуславливает жесткость воды. При действии на В массой 25,02г избытка концентрированной серной кислоты с выходом 89% выделяется бесцветный, хорошо растворимый в воде газ Г объемом (н. у.) 10,5дм3. Определите сумму молярных масс (г/моль) веществ А и В.
Установите соответствие между парой веществ и реагентом, позволяющим различить вещества пары. Все реакции
протекают в разбавленном водном растворе.
А) 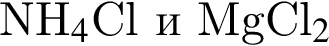
Б) 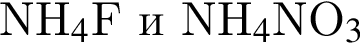
В) 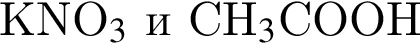
Г) 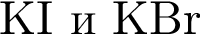
1) ![]()
2) ![]()
3) 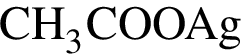
4) 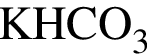
Ответ запишите в виде сочетания букв и цифр, соблюдая алфавитную последовательность букв левого столбца,
например: А1Б4ВЗГ2.
Масса соли, образовавшейся при взаимодействии алюминия с избытком концентрированного раствора гидроксида натрия, составила 2772 г. Рассчитайте химическое количество (моль) электронов, перешедших от атомов алюминия к атомам водорода в результате реакции.
Уксусная кислота широко применяется в качестве консерванта (пищевая добавка Е260). В быту чаще всего используют уксус (массовая доля кислоты 9%, 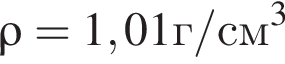 ) или уксусную эссенцию (массовая доля кислоты 70%,
) или уксусную эссенцию (массовая доля кислоты 70%,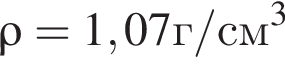 ). Для консервирования овощей требуется 225см3 уксуса. Вычислите, в каком объеме воды (см3) необходимо растворить уксусную эссенцию, чтобы приготовить раствор для консервирования.
). Для консервирования овощей требуется 225см3 уксуса. Вычислите, в каком объеме воды (см3) необходимо растворить уксусную эссенцию, чтобы приготовить раствор для консервирования.
Термохимическое уравнение реакции синтеза аммиака из простых веществ ![]() (г.) +
(г.) + ![]() (г.) =
(г.) = ![]() (г.) + 92 кДж. Смесь азота с водородом общим объемом 400 дм3 (н. у.) с относительной плотностью по водороду 3,6 поместили в реактор для синтеза аммиака. В результате реакции относительная плотность смеси газов по водороду возросла на 19%. Рассчитайте количество теплоты (кДж), выделившейся результате реакции.
(г.) + 92 кДж. Смесь азота с водородом общим объемом 400 дм3 (н. у.) с относительной плотностью по водороду 3,6 поместили в реактор для синтеза аммиака. В результате реакции относительная плотность смеси газов по водороду возросла на 19%. Рассчитайте количество теплоты (кДж), выделившейся результате реакции.
Смесь этилена и паров воды (вода взята в избытке) пропустили над катализатором. В результате реакции с выходом 82 % был получен этанол. После удаления этанола относительная плотность газовой смеси по водороду составила 9,74 (150 °C, 101,3 кПа). Укажите содержание этилена (% по объёму) в исходной газовой смеси.
При взаимодействии фосфорной кислоты с раствором гидроксида натрия образовались кислые соли А и Б, с которыми происходили следующие превращения:
Укажите сумму молярных масс (г/моль) фосфорсодержащих веществ А, Г и Д.

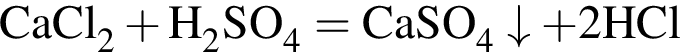
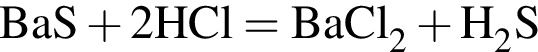
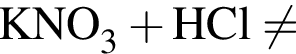
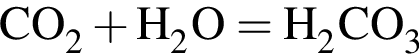
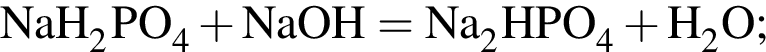
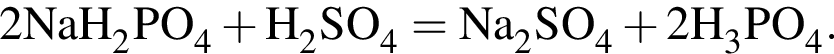
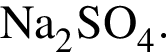
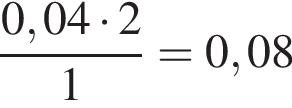 моль/дм3. Текущая концентрация вещества В рассчитывается по формуле C(В) = C0(B) − vB · t, а текущая концентрация вещества D по формуле C(D) = vD · t (v - скорости расходования и образования, соответственно). Найдем время:
моль/дм3. Текущая концентрация вещества В рассчитывается по формуле C(В) = C0(B) − vB · t, а текущая концентрация вещества D по формуле C(D) = vD · t (v - скорости расходования и образования, соответственно). Найдем время: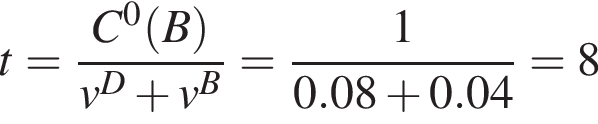 c
c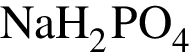 не взаимодействует с обоими веществами, во втором ряду − с азотом. Схемы реакций с веществами в третьем ряду выглядят следующим образом:
не взаимодействует с обоими веществами, во втором ряду − с азотом. Схемы реакций с веществами в третьем ряду выглядят следующим образом: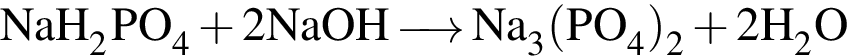 .
.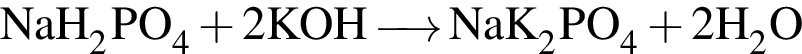 .
.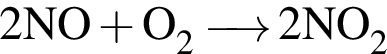
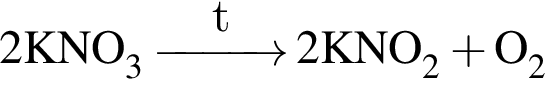
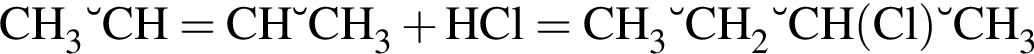 .
.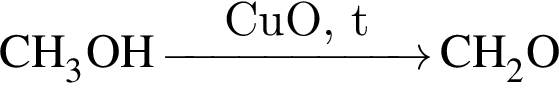
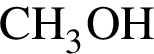
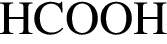
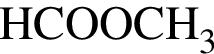
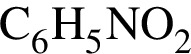 ;
;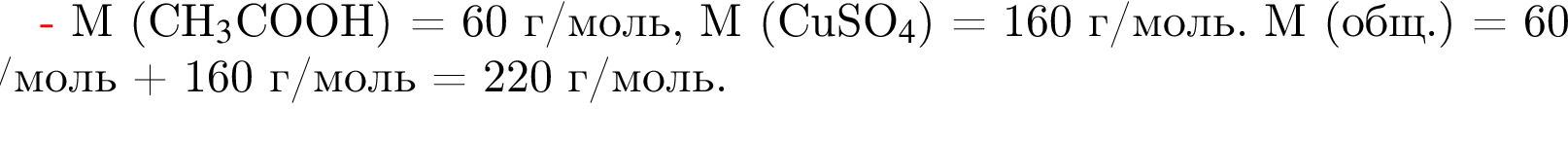
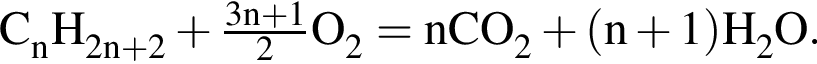
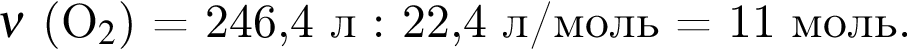

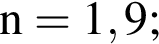
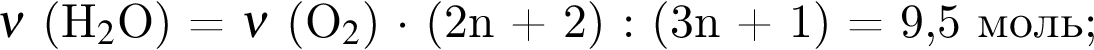
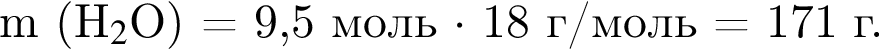
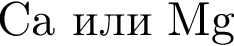 , т. к. они оба в соединениях имеют валентность II, а избыток их катионов обуславливает жесткость воды.
, т. к. они оба в соединениях имеют валентность II, а избыток их катионов обуславливает жесткость воды. 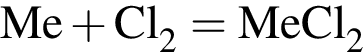 , где
, где 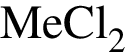 - вещество В.
- вещество В.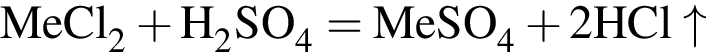 , где
, где 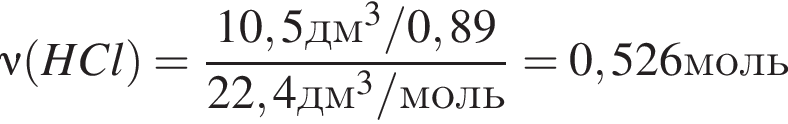
 Откуда
Откуда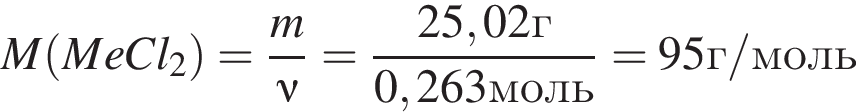

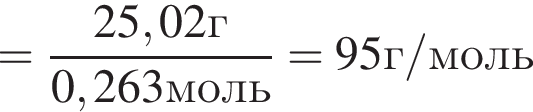

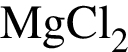 .
.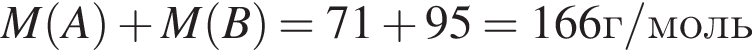

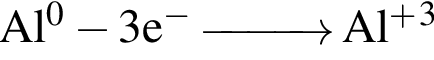
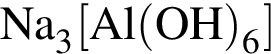 )=2772 г/198 г/моль=14 моль
)=2772 г/198 г/моль=14 моль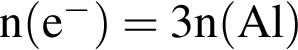 =42 моль
=42 моль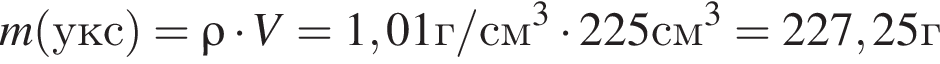


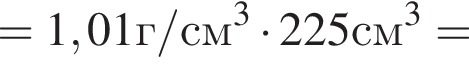

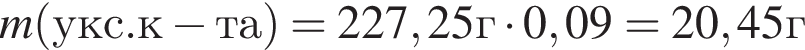
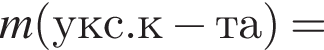
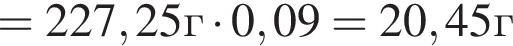
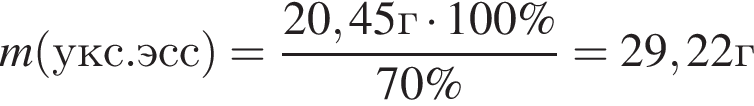
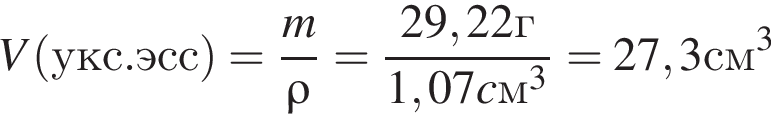
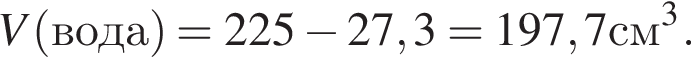 Округлив до целых, получим 198см3.
Округлив до целых, получим 198см3.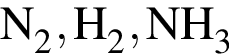 )=17,857−2n моль
)=17,857−2n моль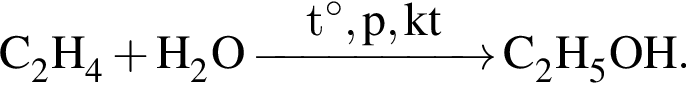
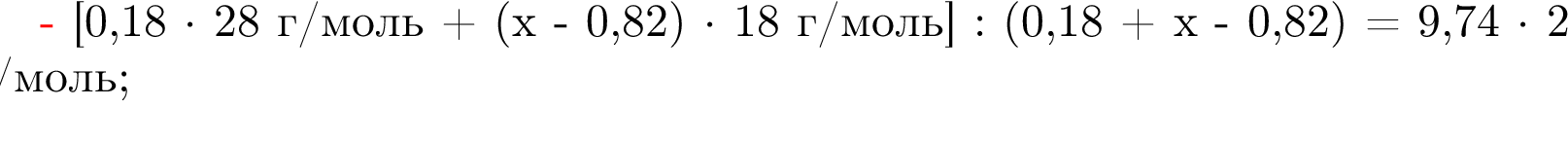
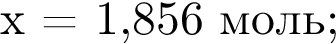
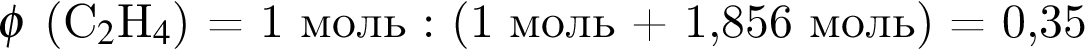 = 35 %
= 35 %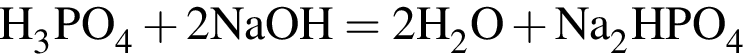 (А);
(А);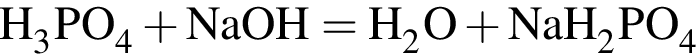 (Б);
(Б);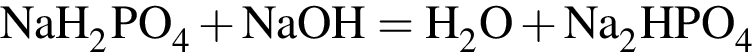 (Б);
(Б);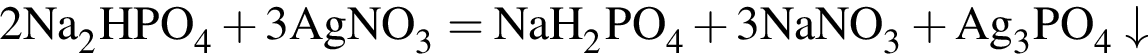 (Г);
(Г);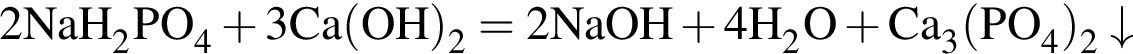 (Д).
(Д).